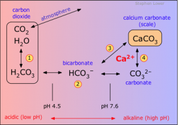
Chi mi aiuta a capire una cosa....
Allora dalla reazione di CO2+H2O ottengo acido carbonico H2CO3. A seguire dalla perdita di protone H+ ottengo bicarbonato e poi ancora dalla perdita di un altro protone carbonati.
La mia domanda è: perché però l' acido perde protoni, a cosa è dovuta questa instabilità?
E poi perché ad esempio l acido carbonico può ritornare acqua e CO2?
Allego un immagine che mi ha aiutato a capire ma non abbastanza.
Inoltre avrei un altra domanda: io ad esempio ho un pH 7.4 ma punto ad un pH acido di 6.5 ok.
Ho un KH che con i cambi da 8 sono arrivato a 4. Questo cosa vuol dire che ho eliminato dei sali? E sto dando prevalenza agli acidi? Ma se sto dando prevalenza agli acidi e quindi ai famosi protoni H+ perché il pH non scende.? Scende ma scende poco ...da 8 che avevo all avvio sono arrivato a 7.4.
Il pH è dato dalla concentrazione di H+ o ioni OH- ma io dalle reazioni degli acidi ottengo sempre protoni e ioni ma che non sono OH- ma ad esempio CO3- vale lo stesso lo ione carbonato per aumentare la basicità dell'acqua?